
笔者于2022年2月向国家药监局申请公开中国三款疫苗在3-17岁人群中“紧急使用”的批准文件、论证文件等文件。此后,国家药监局以《政府信息公开条例》第十四条、第十六条规定为由不公开。在《政府信息公开条例》第十四条中表述的理由包括“公开后可能危及国家安全、公共安全、经济安全、社会稳定的政府信息,不予公开”。
本文以下讲三部分内容:
一、疫苗在3-17岁人群紧急使用疫苗的背景情况。
自2021年6月以来,中国在3-17岁推广接种的疫苗包括“国药北京生物疫苗”、“科兴疫苗”、“国药武汉生物疫苗”三款疫苗。依据相关媒体、单位的介绍,疫苗在3-17岁人群的使用属于尚未达到上市批准的“紧急使用”性质。如,2021年6月11日,人民日报报道“近期,我国有关部门已经批准了3—17岁人群的新冠病毒疫苗紧急使用”;2021年6月11日,国家卫生健康委疾控局二级巡视员崔钢表述:“国家有关部门已经批准了3—17岁人群,可以开展新冠病毒灭活疫苗的紧急使用”;2021年7月18日,中央广播电视总台采访国药集团中国生物首席科学家、副总裁张云涛,其表述:“现在3-17岁只是紧急使用新冠疫苗,还没有批准附条件上市,后续我们会提供更多数据支持达到附条件上市的要求。”
“紧急使用”是《疫苗管理法》规定的疫苗未经上市批准情况下紧急的使用方式。《疫苗管理法》第二十条第二款规定“出现特别重大突发公共卫生事件或者其他严重威胁公众健康的紧急事件,国务院卫生健康主管部门根据传染病预防、控制需要提出紧急使用疫苗的建议,经国务院药品监督管理部门组织论证同意后可以在一定范围和期限内紧急使用。”
上述规定说明以下几个问题:
第一,紧急使用需要首先经过国务院卫生健康主管部门(也就是国家卫健委)“根据传染病预防、控制需要提出紧急使用的建议”,如果国务院卫生健康主管部门并没有提出建议,药品监督管理部门不能自行启动紧急使用疫苗批准程序;
第二,国务院药品监督管理部门应当组织论证对疫苗的紧急使用;
第三,最终同意紧急使用疫苗的单位是药品监督管理部门;
第四,药品监督管理部门同意紧急使用的同时需要确定“使用范围”和“期限。”
经过笔者查询,并未发现国家药监局主动公开三款疫苗在3-17岁人群中紧急使用的同意批准信息。这个情况相当不寻常,因为这三款疫苗在18岁以上人群中附条件批准上市的信息在国家药监局官网有主动公开,而为什么在3-17岁人群中紧急使用却不主动公开呢?
二、笔者申请国家药监局公开3-17岁人群紧急使用疫苗的批准文件相关情况。
2022年2月15日,笔者向国家药监局申请公开三款疫苗的以下三项信息:
1、上述三款疫苗在3岁至17岁人群中紧急使用的全部批准文件或同意文件(包括使用范围和使用期限)。
2、上述三款疫苗在3岁至17岁人群中紧急使用的全部论证文件。
3、国务院卫生健康主管部门根据传染病预防、控制需要提出紧急使用上述三款疫苗的全部建议文件。
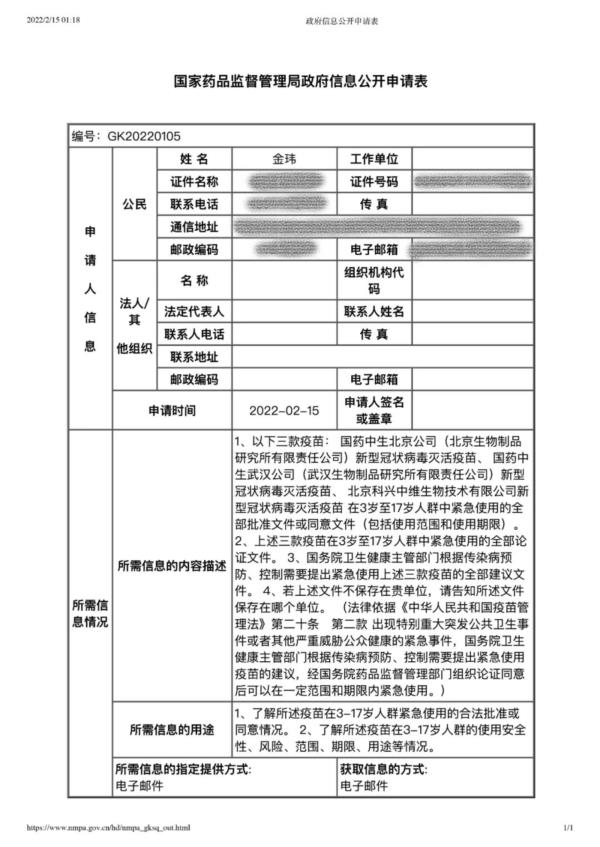
2022年2月25日,国家药监局向我送达了《政府信息公开告知书》。其对于我的申请的答复是:“根据《政府信息公开条例》第十四条、第十六条规定,不予公开。”

笔者查阅的《政府信息公开条例》第十四条、第十六条,内容如下:
第十四条依法确定为国家秘密的政府信息,法律、行政法规禁止公开的政府信息,以及公开后可能危及国家安全、公共安全、经济安全、社会稳定的政府信息,不予公开。
第十六条行政机关的内部事务信息,包括人事管理、后勤管理、内部工作流程等方面的信息,可以不予公开。行政机关在履行行政管理职能过程中形成的讨论记录、过程稿、磋商信函、请示报告等过程性信息以及行政执法案卷信息,可以不予公开。法律、法规、规章规定上述信息应当公开的,从其规定。
三、笔者对于国家药监局不公开上述信息的理由的疑问。
国家药监局以《政府信息公开条例》第十四条、第十六条为由拒绝公开。第十四条包含了6种不公开情形;第十六条包含了两类不公开情形,因此国家药监局所列的法条理由其实是一个“理由范围”;并没有明确不公开的具体的事实和理由,而是要申请人自己去推测。笔者尚未查找到申请公开的信息属于国家秘密或者法律法规规定不能公开的依据,所以笔者认为国家药监局不公开批准文件的主要的理由可能是第十四条所述“公开后可能危及国家安全、公共安全、经济安全、社会稳定的政府信息”。如果真是这个理由,对此问题,笔者有下列的疑问:
疑问1、公开对3-17岁人群紧急使用疫苗的同意或批准文件为什么会危及社会稳定?
行政机关同意文件或批准文件是行政机关依法行政的法律文件,也是下属各单位,以及其他单位、民众可以信赖政府确实下达了同意或批准的凭证。如果谁都看不到这份文件,无法确信药监局确实同意批准“紧急使用”疫苗。不要忘记,曾经某市民众“以为”封/尘/两个月,事后政府主张并无政府官方文件,不存在封/尘/,待在家里都是民众自愿。所以这份文件是很有必要公开以证实确有其事,历经合法手续。
为什么公开合法手续,会危及社会稳定呢?
疑问2、不公开批准文件是否和“知情”原则相违背?
国务院应对新型冠状病毒肺炎疫情联防联控机制综合组制定的《关于印发新型冠状病毒肺炎防控方案(第九版)的通知》明确要求,疫苗接种要“坚持知情、同意、自愿原则”。而在3-17岁人群紧急使用疫苗的同意或批准文件,是民众应当知道最基本的情况。若不掌握这个同意或批准文件的全面、完整、准确的信息,民众何以能够“知情”?
现在这个文件不公开,是否和知情原则相违背?
疑问3、公开可能危及社会稳定是指批准或者论证文件中描述的疫苗的副作用或风险的信息吗?
如前所述,所述三款疫苗的性质是未上市的紧急使用,所以疫苗可能的副作用或者可能的风险当然有可能存在。如果批准文件或者论证文件中描述了疫苗的副作用或风险,笔者认为,当然属于民众应当知晓的内容。若能知晓这些信息,民众才能充分地知道使用疫苗的风险的大小,充分自愿地选择接种还是不接种,医疗机构才能对接种疫苗后的反应作出更为准确判断,这样才能使得民众有稳定的心理预期,让医疗机构能有更好的掌握应对方法,恰恰有利于社会稳定。而不公开这信息,笔者以为恰恰不利于社会稳定。
药监局指的公开可能危及稳定,是指这部分疫苗副作用或风险信息吗?如果不是这部分信息,是指什么其他信息公开后可能危及社会稳定?
疑问4、对3-17岁人群“紧急使用”疫苗的期限和范围,我们如何知晓?
《疫苗管理法》第二十条第二款规定,“紧急使用”疫苗,是需要“经国务院药品监督管理部门组织论证同意后可以在一定范围和期限内紧急使用。”所以可以知道,对所述疫苗的紧急使用等同意和批准,一定是有期限和范围的要求的。现在药监局不公开批准文件,我们也就无从知晓紧急使用的真实的期限和范围。
期待国家药监局早日主动公开上述信息。
让民众得以充分“知情”的情况下,自愿选择。


